Link para boletim completo: https://www.gov.br/saude/pt-br/centrais-de-conteudo/publicacoes/boletins/epidemiologicos/edicoes/2023/boletim-epidemiologico-volume-54-no-10/@@download/file
Resumo:
INTRODUÇÃO
A vacinação contra a covid-19 foi iniciada na segunda quinzena de janeiro de 2021, com as vacinas AstraZeneca/Fiocruz e Sinovac/Butantan em grupos populacionais considerados de maior risco. Em maio do mesmo ano, houve a inclusão de uma terceira vacina do laboratório Pfizer/Wyeth e em junho foi introduzida no Plano Nacional de Operacionalização da Vacinação contra a Covid-19 (PNO) a vacina Janssen, de tal forma que atualmente (JUN/2023) estão disponíveis quatro imunobiológicos contra a doença.
Em fevereiro de 2023, foi iniciada a Campanha Nacional de Vacinação contra a Covid-19 utilizando a vacina Pfizer/Wyeth bivalente para toda a população de 6 meses a 59 anos não vacinada ou com esquemas incompletos. Atualmente, a vacinação contra a covid-19 no Brasil é indicada para a população a partir de 6 meses de idade, com as formulações adultas já citadas e a formulação pediátrica da vacina Pfizer/Wyeth (a partir dos 6 meses a 11 anos de idade) e a vacina Sinovac/Butantan, que está indicada a partir dos 3 anos de idade.
Todas as vacinas ofertadas pelo Programa Nacional de Imunizações (PNI) são seguras, possuem autorização de uso pela Agência Nacional de Vigilância Sanitária (Anvisa) e passam por um rígido processo de avaliação de qualidade pelo Instituto Nacional de Controle de Qualidade em Saúde (INCQS) da Fundação Oswaldo Cruz, instituição responsável pela análise de qualidade dos imunobiológicos adquiridos e distribuídos pelo Sistema Único de Saúde (SUS).
Previamente à sua introdução, as vacinas COVID-19 passaram por todas as fases de estudos pré-clínicos e estudos clínicos (fase I, II e III), estando atualmente na fase IV de avaliação clínica, denominada fase pós-implantação, onde é realizada a farmacovigilância de vacinas e outros imunobiológicos com o monitoramento dos Eventos Supostamente Atribuíveis à Vacinação ou Imunização (ESAVI) de forma a identificar possíveis eventos adversos raros (entre 1 evento a cada mil doses a 1 evento a cada 10 mil doses) e muito raros (menos de 1 evento a cada 10 mil doses).
É fundamental o monitoramento da efetividade e da segurança das vacinas durante a campanha, onde a detecção e a notificação oportuna dos ESAVIs COVID-19 permitem, juntamente com a contenção do agravo, não apenas o acolhimento dos indivíduos afetados, mas também a credibilidade e a segurança do programa de vacinação.
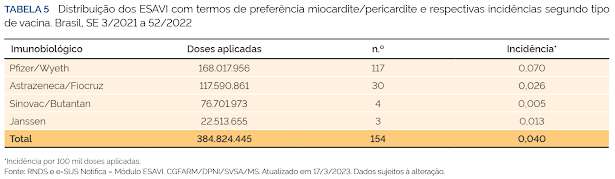
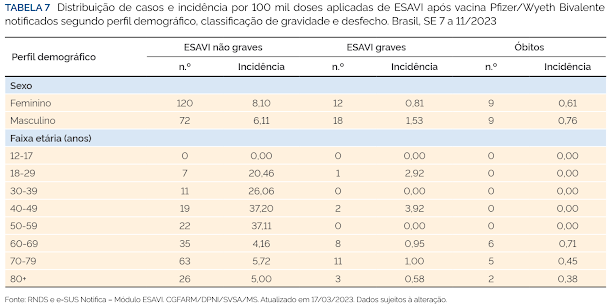
Este Boletim Epidemiológico descreve os resultados do monitoramento da segurança das vacinas COVID-19 ofertadas no Brasil até a semana epidemiológica (SE) n.º 11 de 2023, assim como, de forma mais detalhada, os ESAVIs ocorridos após a vacina Pfizer/Wyeth Bivalente BA.4/BA.5, os óbitos por ESAVI ocorridos em menores de 18 anos e ESAVIs notificados com descrição de Miocardite/Pericardite.
(Considerando-se a complexidade do trabalho que compara as diversas vacinas e faixas etárias, sugere-se a leitura completa do mesmo, a partir do link fornecido. Abaixo algumas tabelas importantes e conclusões do estudo.)
A vacinação contra a covid-19 avança a passos largos em todo país, tendo sido administradas, no período analisado, cerca de 510 milhões de doses em todo o Brasil, com a consequente redução do número de casos, internações e óbitos pela doença. Ao vacinar um número tão grande de indivíduos, é esperada a notificação de um elevado número de ESAVI, incluindo EG. No entanto, destaca-se que, após a investigação adequada, apenas uma pequena parcela destes eventos teve qualquer relação causal com a vacinação. Ressalta-se ainda que a vacinação contra a covid-19 ocorreu em vigência de elevada incidência de casos de covid-19, de tal forma que um número expressivo de indivíduos pode ter sido vacinado no período de incubação do vírus SARS-CoV-2, levando a notificação de número expressivo de ESAVI coincidentes com a vacinação.
A maioria dos ESAVIs notificados com as vacinas COVID-19 são ENG, apresentando uma incidência de cerca de 98,25 eventos/100 mil doses aplicadas. Em relação aos ESAVIs graves, apenas 0,005% do total de doses aplicadas no período analisado evoluiu para essa classificação, ou seja, a maciça maioria desses eventos não teve qualquer relação causal com a vacinação. Além disso, apesar de 4.458 notificações conterem o desfecho óbito, após revisão das avaliações de causalidade e encerramento pela esfera federal e/ou Cifavi, apenas 50 óbitos tiveram relação causal consistente com a vacinação, isto é, 0,013 casos/100 mil doses aplicadas.
Uma publicação do Imperial College London, estimou que a vacinação evitou no Brasil entre 700 a 880 mil mortes até o final de 2021, ou seja, para cada óbito por ESAVI com relação causal consistente com a vacinação, entre 43.750 a 55.000 outros óbitos foram evitados pela vacinação11. Ressalta-se, ainda, que estas foram estimativas conservadoras, tendo em vista que a estimativa de óbitos evitados não incluiu o pico epidêmico ocorrido em 2022, momento em que a incidência de casos graves e óbitos pela covid-19 teve sua maior ocorrência na população não vacinada desde o início da pandemia no Brasil.
Ainda, o impacto da covid-19 vai muito além do risco de morte ou internações, podendo levar a complicações tais como: tromboses venosas, miocardite e pericardite, síndromes neurológicas como a síndrome de GuillainBarré, encefalite e doenças desmielinizantes, hemorragias cerebrais, arritmia, infarto agudo do miocárdio (IAM), embolia pulmonar, entre outros. Isso posto, os dados aqui apresentados denotam o excelente perfil de benefício versus risco da vacinação contra a covid-19. No entanto, como qualquer outro medicamento, não se pode descartar totalmente o risco de ocorrência deEG. É importante destacar, no entanto, que estes eventos são muito raros, ocorrendo em média um (1) caso a cada 100 mil doses aplicadas, apresentando um risco significativamente inferior ao risco de complicações pela própria covid-19.
Os EG notificados com provável ou possível, mas não necessariamente com relação causal confirmada com a vacinação após o seu uso em larga escala foram principalmente: reações de hipersensibilidade graves, síndrome de trombose com trombocitopenia (STT) relacionados as vacinas da plataforma de vetor viral (Astrazeneca e Janssen), eventos de pericardite e miocardite com as vacinas de RNAm e a síndrome de Guillain-Barré.
Os dados apresentados neste Boletim devem ser considerados como sujeitos a alterações, devido
ao caráter dinâmico e com constantes atualizações da vigilância epidemiológica de ESAVI. O MS segue
monitorando a ocorrência de ESAVI com as vacinas COVID-19 administradas no país. Até o momento, os dados indicam que essas vacinas apresentam excelente perfil de benefício versus risco, tendo gerado um impacto extremamente positivo na saúde da população brasileira, com a redução expressiva dos casos, internações e óbitos pela doença.
Uma limitação clássica da vigilância passiva de ESAVI é a possibilidade da subnotificação. Na farmacovigilância de rotina, a taxa de notificação representa em média 6 a 10% dos casos reais de ESAVIs, e a subnotificação pode ser maior para casos não graves, segundo alguns autores.
Isto, por sua vez, dificulta a mensuração da real incidência de ESAVIs nos estudos epidemiológicos.16
Desta forma, aos profissionais de saúde, ressalta-se a importância da notificação e da investigação aprofundada dos ESAVIs ocorridos em associação temporal com as vacinas COVID-19, para uma adequada apreciação do caso e consequentemente avaliação de risco.
Às vigilâncias estaduais e municipais, recomenda-se ações orientativas e de educação continuada de forma a esclarecer e atualizar os profissionais que trabalham nas vigilâncias e aqueles de estabelecimentos de saúde que são porta de entrada para casos de ESAVI, e com isso melhorar a sensibilidade para a notificação de casos com relação temporal com imunobiológicos, assim como a qualidade e a oportunidade das investigações para avaliações de causalidade e encerramentos adequados.

Nenhum comentário:
Postar um comentário